Giải bài tập hoá 9, giải hóa 9 chi tiết, dễ hiểu
Lớp 2 - kết nối tri thức
Lớp 2 - Chân trời sáng tạo
Lớp 2 - Cánh diều
Tài liệu tham khảo
Lớp 3Sách giáo khoa
Tài liệu tham khảo
Sách VNEN
Lớp 4Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Lớp 5Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Lớp 6Lớp 6 - kết nối tri thức
Lớp 6 - Chân trời sáng sủa tạo
Lớp 6 - Cánh diều
Sách/Vở bài bác tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 7Sách giáo khoa
Sách/Vở bài bác tập
Đề thi
Chuyên đề và Trắc nghiệm
Lớp 8Sách giáo khoa
Sách/Vở bài tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 9Sách giáo khoa
Sách/Vở bài bác tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 10Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 11Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Chuyên đề & Trắc nghiệm
Lớp 12Sách giáo khoa
Sách/Vở bài xích tập
Đề thi
Chuyên đề và Trắc nghiệm
ITNgữ pháp tiếng Anh
Lập trình Java
Phát triển web
Lập trình C, C++, Python
Cơ sở dữ liệu
Bạn đang xem: Giải bài tập hoá 9, giải hóa 9 chi tiết, dễ hiểu

Các dạng bài bác tập chất hóa học lớp 9Chương 1: các loại hợp hóa học vô cơChương 2: Kim loạiChương 3: Phi kim. Sơ sài về bảng tuần hoàn những nguyên tố hóa họcChương 4: Hiđrocacbon. Nhiên liệuChương 5: Dẫn xuất của Hiđrocacbon. Polime
Các dạng bài tập hóa học 9 Chương 5: Dẫn xuất của Hiđrocacbon - Polime cực hay, có lời giải
Xem thêm: Bật Mí Cách Chăm Lan Hồ Điệp Ra Hoa Rực Rỡ, Kỹ Thuật Trồng Cây Hoa Lan Hồ Điệp Trong Chậu
Trang trướcTrang sau
Để học giỏi Hóa học lớp 9, phần bên dưới tổng hợp định hướng và bài bác tập trắc nghiệm (có đáp án) hóa học lớp 9 Chương 5: Dẫn xuất của Hiđrocacbon. Polime. Chúng ta vào tên dạng hoặc Xem cụ thể để xem những chuyên đề chất hóa học 9 tương ứng.
Mục lục Hóa 9 Chương 5: Dẫn xuất của Hiđrocacbon. Polime
I. Kim chỉ nan & Trắc nghiệm theo bài bác học
II. Các dạng bài xích tập
Phương pháp giải bài bác tập về độ rượu
Lý thuyết và phương thức giải
I. Định nghĩa:
Độ rượu là số ml rượu nguyên hóa học trong 100 ml hỗn hợp rượu với nước.
II. Công thức yêu cầu nhớ
- phương pháp tính độ rượu
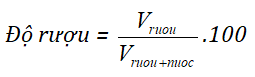
- Công thức khối lượng riêng
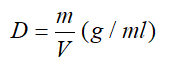
III. Cách thức giải
- bước 1: xử trí dữ kiện đề bài bác cho.
- cách 2: Tính Vrươu, Vruou+nuoc.
- cách 3: Tính độ rượu cần tìm.
Bài tập vận dụng
Bài 1: kết hợp m gam ancol etylic (D=0,8 gam/ml) vào 216 ml nước (D=1 gam/ml) chế tạo thành dung dịch A. Mang lại A công dụng với mãng cầu dư nhận được 170,24 lit (đktc) khí H2. Hỗn hợp A tất cả độ rượu bằng bao nhiêu?
Hướng dẫn:
Na + C2H5OH → C2H5ONa + 1/2H2
----------x-------------x-----------x/2
Na + H2O → NaOH + 1/2H2
--------y---------y---------y/2
Theo bài xích ta gồm DH2O = 1 gam/ml
⇒ mH2O = 216 gam ⇒ nH2O = 216/18 = 12 mol = y
Mà nH2 = x/2 + y/2 = 170,24/22,4 = 7,6 mol
⇒ nC2H5OH = x = 3,2 mol
⇒ mC2H5OH = 3,2.46 = 147,2 gam
⇒ VC2H5OH = m/D = 147,2/0,8 = 184 ml
⇒ Vdd = 184 + 216 = 400 ml
⇒ D = 184.100/400 = 46 độ
Bài 2: Lên men 1 lit ancol etylic 23 độ thu được giấm ăn. Biết năng suất lên men là 100% và cân nặng riêng của ancol etylic là 0,8 gam/ml. Khối lượng axit axetic vào giấm là bao nhiêu?
Hướng dẫn:
Vruou= Độ rượu.Vdd = 0,23.1000 = 230 ml
⇒ mrượu = Vrượu.D = 230.0,8 = 184 gam
C2H5OH + O2 → CH3COOH + H2O
46 --------------------------------60
184 -------------------------→ m = ?
⇒ mCH3COOH = 184.60/46 = 240 gam
Cách giải bài xích tập phản ứng tráng gương của glucozo
Lý thuyết và phương thức giải
- Phương trình phản nghịch ứng:
C6H12O6 + Ag2O → C6H12O7 + 2Ag
Nhớ: 2nC6H12O6 = nAg
- phương thức chung:
+ so sánh xem đề cho gì và hỏi gì
+ Tính n của hóa học mà đề cho. Tính số mol của chất đề hỏi ⇒ khối lượng của hóa học đề hỏi
Bài tập vận dụng
Bài 1: Đun lạnh 250 gam hỗn hợp glucozơ với dung dịch AgNO3 /NH3 thu được 15 gam Ag, nồng độ của dung dịch glucozơ là bao nhiêu?
Hướng dẫn:
nAg = 15/108 mol
C6H12O6 + Ag2O → C6H12O7 + 2Ag (1)
Theo pt (1) ta bao gồm nC6H12O6 = ½.nAg = ½.(15/108) = 0,07 mol
mctC6H12O6 =0,07 .180 = 12,5g
C% C6H12O6 = (12,5/250).100% = 5%
Bài 2: Để tráng bạc đãi một dòng gương soi, tín đồ ta phải đun rét dung dịch đựng 36g glucozơ với số lượng vừa đủ dung dịch AgNO3 trong amoniac. Trọng lượng bạc vẫn sinh ra dính vào mặt kính của gương và khối lượng AgNO3 cần cần sử dụng lần lượt là bao nhiêu (biết những phản ứng xẩy ra hoàn toàn)
Hướng dẫn:
nglucozo = 36/180 = 0,2 mol
C6H12O6 + Ag2O → C6H12O7 + 2Ag
0,2 …………….. →………………0,4 mol
mAg = 0,4.108 = 43,2g
BTNT Ag ta có: nAgNO3 = nAg = 0,4 mol
mAgNO3 = 0,4.(108+14+16.3) = 68g
Cách giải bài tập phản bội ứng lên men của glucozo
Lý thuyết và phương pháp giải
- Phương trình phản nghịch ứng:
C6H12O6 −to, men rượu→ 2C2H5OH + 2CO2
- phương thức chung:
+ đối chiếu xem đề cho gì và hỏi gì
+ Tính n của chất mà đề cho. Tính số mol của chất đề hỏi ⇒ khối lượng của chất đề hỏi
Bài tập vận dụng
Bài 1: Lên men dung dịch chứa 300 gam glucozơ chiếm được 92 gam ancol etylic. Hiệu suất quá trình lên men tạo ra thành ancol etylic là bao nhiêu?
Hướng dẫn:
netylic = 92/46 = 2 mol
C6H12O6 −to, men rượu→ 2C2H5OH + 2CO2 1…………………………….2 mol
Hiệu suất quy trình lên men sinh sản thành ancol etylic là :
H = (1.180/300) .100% =60%
Bài 2: Lên men trọn vẹn m gam glucozơ thành ancol etylic. Toàn bộ khí CO2 sinh ra trong quy trình này được kêt nạp hết vào hỗn hợp Ca(OH)2 dư tạo ra 40 gam kết tủa. Nếu hiệu suất của quá trình lên men là 75% thì quý giá của m là bao nhiêu?
Hướng dẫn:
C6H12O6 −to, men rượu→ 2C2H5OH + 2CO2(1)
CO2 + Ca(OH)2 → CaCO3 + H2O(2)
Ta có: nCaCO3 = nCO2 = 40/100 = 0,4 mol
Theo pt (1) ta có: nC6H12O6(ly thuyet) = (1/2).nCO2 = (1/2).0,4 = 0,2 mol
H = 75% ⇒ nC6H12O6(thuc te) = (0,2/75).100 = 0,267 mol
⇒ m = 0,267.180 = 48g
Giới thiệu kênh Youtube huroji.com
CHỈ CÒN 250K 1 KHÓA HỌC BẤT KÌ, huroji.com HỖ TRỢ DỊCH COVID
Phụ huynh đk mua khóa đào tạo và huấn luyện lớp 9 mang lại con, được khuyến mãi miễn giá thành khóa ôn thi học tập kì. Phụ huynh hãy đk học demo cho bé và được support miễn phí. Đăng cam kết ngay!















